
Анализ отечественной и зарубежной литературы показывает стабильный рост показателей заболеваемости раком шейки матки и смертности от него у женщин репродуктивного возраста. Несмотря на совершенствование скрининговых программ во всем мире, доля больных с запущенными формами остается высокой и достигает 32%.
Среди всей онкопатологии заболевания женской репродуктивной системы в РФ составляют 18,2 %. При этом рак шейки матки в общей структуре онкологической заболеваемости занимает 4-е ранговое место, а среди органов репродуктивной системы – 2-е место (13,3 %), уступая раку молочной железы (47,8 %). Данные показатели отражают малую эффективность медицинских и социальных программ, направленных на снижение заболеваемости раком шейки матки, а также на повышение выживаемости и качества жизни пациенток с данной патологией.
Ситуация в мире
Рак шейки матки (РШМ), согласно данным Международного агентства по изучению рака, занимает 2-е ранговое место среди онкологических заболеваний женской репродуктивной системы, уступая по частоте лишь раку молочной железы (РМЖ), что обусловливает актуальность проблемы данного заболевания как в медицинском, так и в социальном аспекте [1–4].
В 2020 г. в мире было зарегистрировано 604 127 новых случаев РШМ и 341 831 случаев смерти от этого заболевания. Стандартизированный показатель заболеваемости в 2020 г. составил 13,3 случая на 100 тыс. женщин, а стандартизированный показатель смертности – 7,2 на 100 тыс. женщин [5–9].
Более половины всех случаев впервые выявленного РШМ в 2020 г. пришлось на развивающиеся страны Азии, Африки. В 23 странах мира РШМ является наиболее часто выявляемым онкологическим заболеванием и в 36 странах – основной причиной смерти. На рис. 1 приведена географическая вариабельность заболеваемости РШМ и смертности от него в различных странах [5–11].
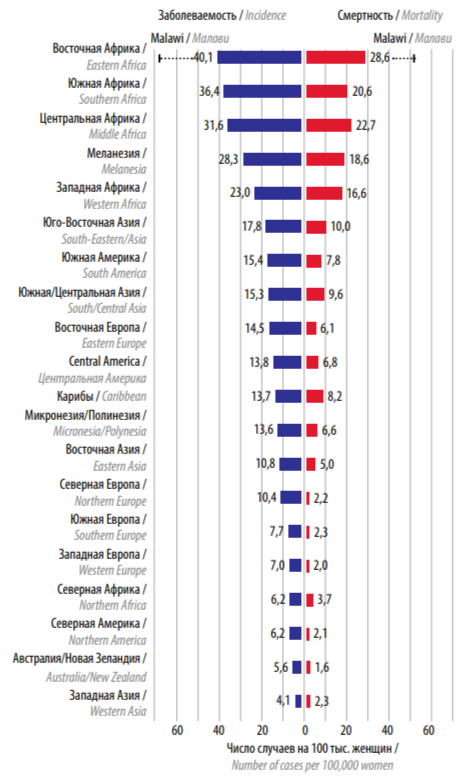
Рис. 1. Данные мировой статистики по заболеваемости раком шейки матки и смертности от него в 2020 г.
При РШМ существует четкий социально-экономический градиент, при этом отмечено снижение показателей по мере увеличения так называемого индекса человеческого развития. Более высокая заболеваемость (18,8 на 100 тыс.) и смертность при РШМ (12,4 на 100 тыс.) зафиксирована в странах с более низким индексом человеческого развития по сравнению со странами с высоким уровнем этого индекса (стандартизированный показатель составляет 11,3 на 100 тыс. для заболеваемости и 5,2 на 100 тыс. для смертности) [8]. Это неравенство существует даже в странах с высоким уровнем дохода, таких как США, где уровень смертности от РШМ в 2 раза выше среди женщин, проживающих в районах с высоким уровнем бедности, по сравнению с женщинами, проживающими в районах с относительно низкой частотой бедности [12–14].
В 2020 г. выявлено стабильное снижение заболеваемости РШМ в большинстве стран мира с высоким уровнем дохода и развитыми службами популяционного скрининга и лечения, таких как Швеция, Австралия и Великобритания. Напротив, заболеваемость выросла в некоторых странах Восточной Африки и Восточной Европы, в частности в Колумбии, Индии и Уганде (см. рис. 1) [5, 12–14].
Высокие показатели заболеваемости в странах третьего мира обусловлены социально-экономическими факторами и отсутствием скрининговых программ, направленных на раннее выявление, профилактику и лечение предраковых заболеваний [13–19].
Рак шейки матки в России
По данным Всемирной организации здравоохранения (ВОЗ), Российская Федерация входит в число 7 стран с наибольшим числом распространенных злокачественных новообразований – РШМ, удельный вес которого составляет 5,8 % в структуре общей онкологической заболеваемости.
За период с 2015 по 2020 г. в РФ выявлено 44 214 новых случаев РШМ, из них 12 252 – в 2020 г., и зарегистрировано 7550 летальных случаев [5, 6, 11, 19–23]. В 2020 г. РШМ занял 5-е ранговое место среди злокачественных заболеваний у женщин, составляя 5,2 % и занимая 3-е место среди злокачественных новообразований репродуктивной системы, уступая лишь РМЖ (21,7 %) и раку тела матки (8 %) [22–24].
Из приведенных показателей следует, что РШМ в России занимает одну из лидирующих позиций в структуре онкологической заболеваемости и смертности.
Статистические показатели заболеваемости РШМ и смертности от него женского населения России в 2011–2020 гг., представленные в работе А.Д. Каприна и соавт. в 2021 г. [23], позволили структурировать имеющиеся данные в диаграмму, отражающую абсолютное число впервые установленных диагнозов РШМ и абсолютное число умерших от РШМ (рис. 2). Согласно представленным данным, наблюдается неуклонный рост впервые выявленных случаев заболевания за последнее десятилетие: в 2011 г. было зарегистрировано 14 834 новых случая РШМ, в 2019 г. – 17 503. Вместе с тем отмечено некоторое снижение этого показателя в 2020 г. – 15 500 случаев.
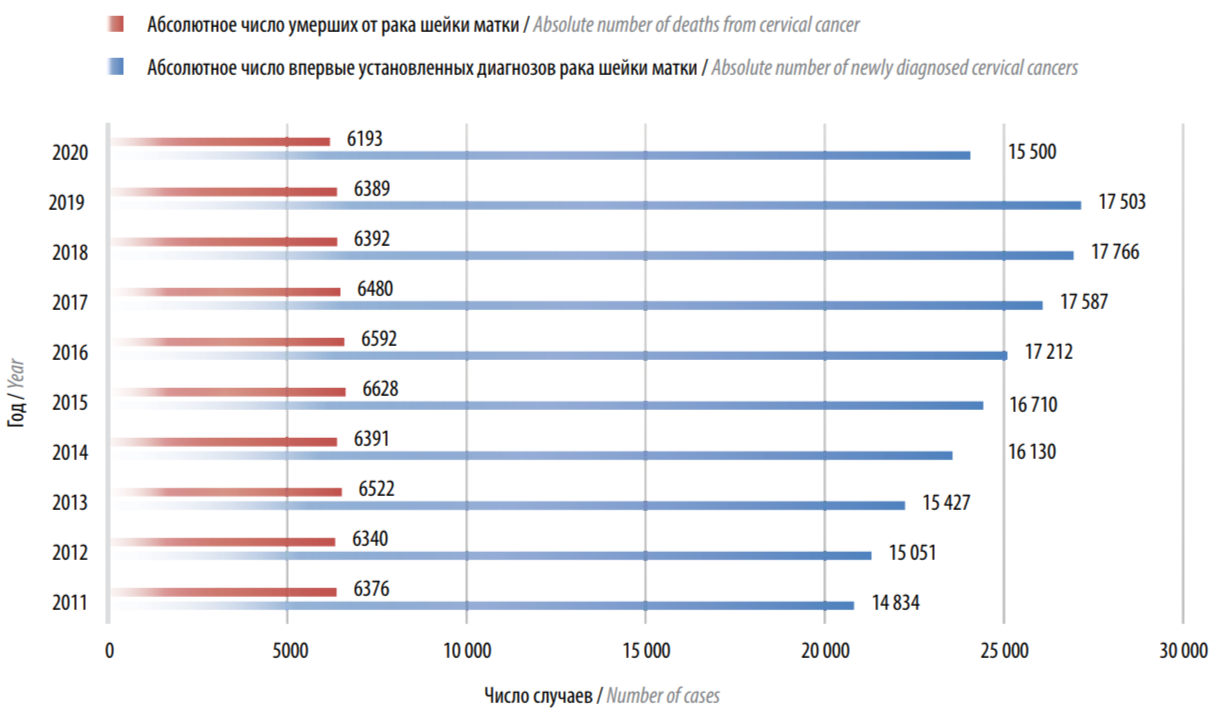
Рис. 2. Диаграмма заболеваемости раком шейки матки и смертности от него женского населения России в 2011–2020 гг. [22, 23]
В динамике «грубый» показатель годовой заболеваемости за период с 2010 по 2020 г. повысился с 19,3 до 19,75 на 100 тыс. населения. За этот период суммарный прирост составил 13,63 % со среднегодовым темпом 1,27 %. Стандартизированный показатель заболеваемости за период с 2010 по 2019 г. повысился с 13,71 до 15,38 на 100 тыс. населения, однако в 2020 г. отмечено снижение показателя до 13,67 на 100 тыс. населения [23].
Абсолютное число умерших от РШМ сохраняет свою стабильность в 2010–2020 гг., превышая 6100–6200 случаев в год. Интересно, что этот показатель полностью совпадает по данным 2010 и 2020 гг. – 6193 случая в год [23].
Интересные данные (рис. 3) получены при структурировании соотношения кумулятивного риска развития злокачественного новообразования и риска смерти от РШМ за 2011–2020 гг. [23]. Как показывает анализ, риск смерти от РШМ оставался практически неизменным в 2011–2017 гг. (0,54–0,56), в 2020 г. составил 0,51; однако риск развития РШМ значительно увеличился с 2011 по 2018 г. с 1,35 до 1,56 со снижением данного показателя в 2020 г. до 1,35.
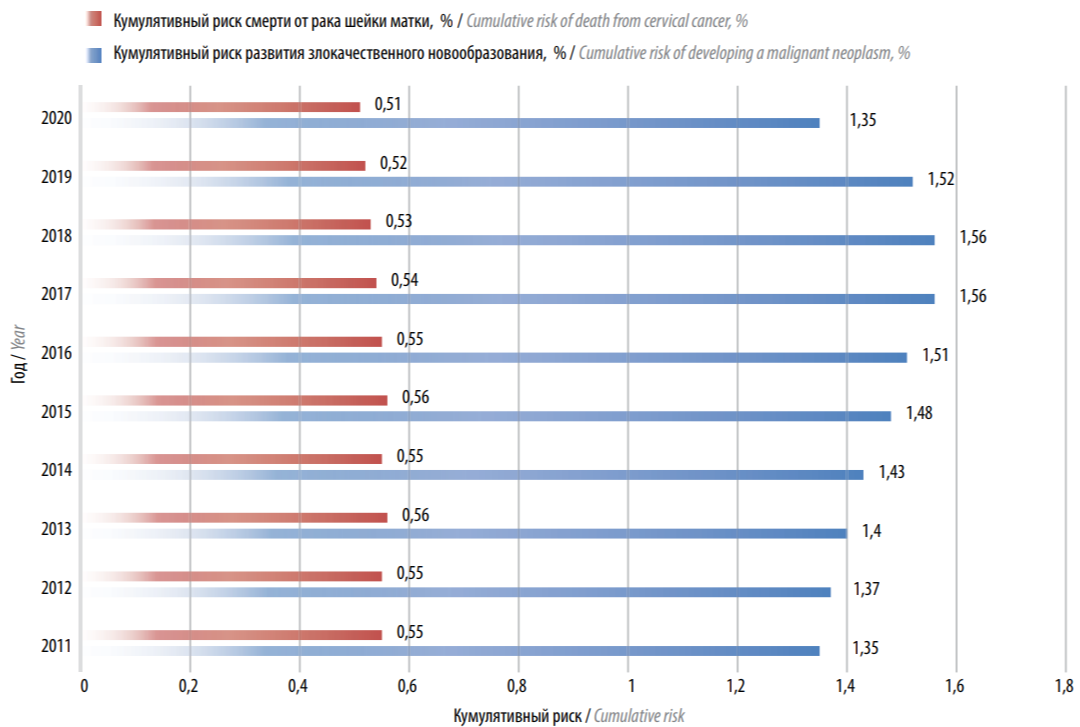
Рис. 3. Соотношение кумулятивного риска развития злокачественного новообразования и риска смерти от рака шейки матки за 2011–2020 гг., % [23]
Средний возраст больных с впервые в жизни установленным диагнозом РШМ за последнее десятилетие практически не изменился и составил в России в 2020 г. 52,5 года. Однако обращает на себя внимание тенденция к повышению уровня заболеваемости РШМ у женщин молодого возраста: здесь максимальный удельный вес зарегистрирован в возрасте до 35 лет – 46,88 %. В возрастной категории 35–44 лет РШМ выявлен у 35,25 %, в перименопаузальном периоде (45–54 года) и постменопаузальном (после 55 лет) – у 18,49 и 18,59 % соответственно (рис. 4) [23, 24].
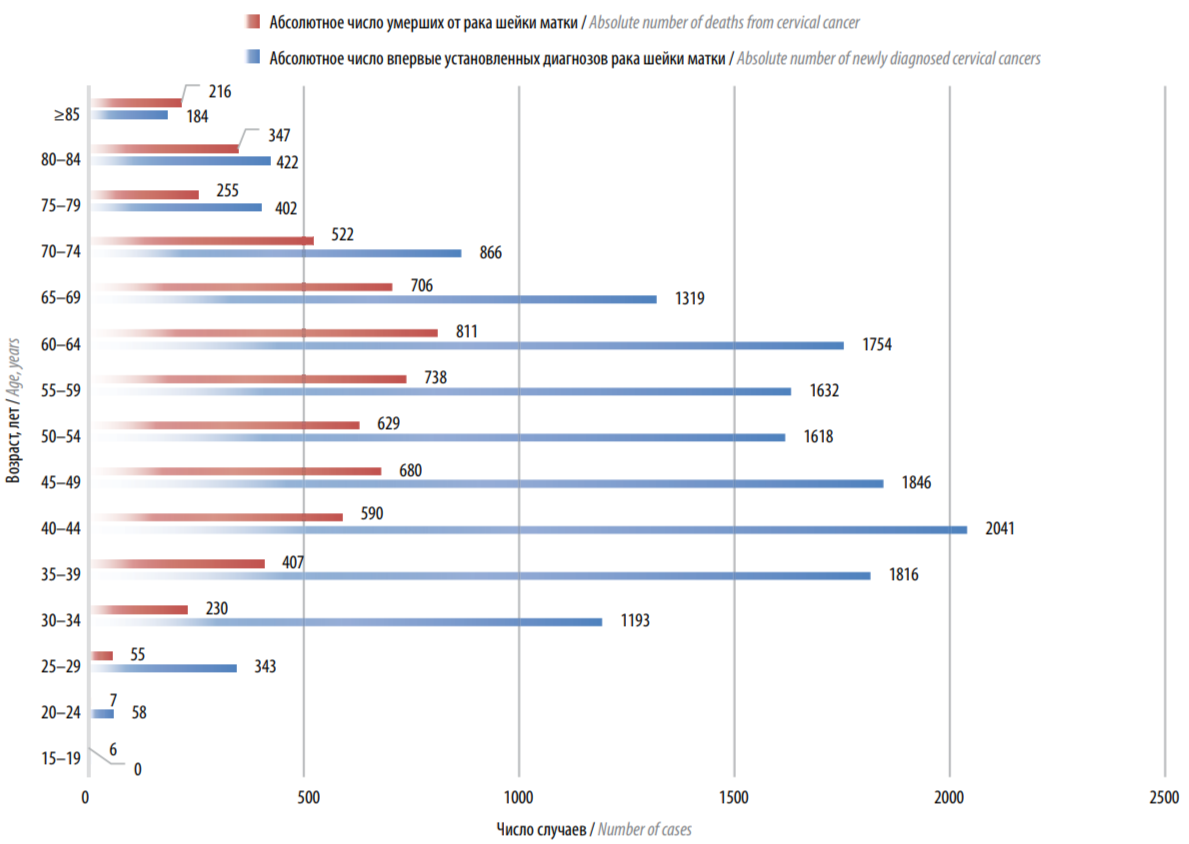
Рис. 4. Соотношение заболеваемости раком шейки матки и смертности от него в возрастных группах женского населения России в 2020 г. [23]
Несмотря на то, что РШМ относится к новообразованиям визуальной локализации, отмечается большое количество выявленных случаев с запущенными формами: в 2020 г. выявлено 33,6 % больных с III–IV стадией, что и обусловливает высокий показатель однолетней летальности – 12,6 % [24–34].
Отмечается стабильность средних возрастных показателей смертности от РШМ у женщин среднего возраста: в 2010 г. – 58,1 года, в 2020 г. – 58,3 года. У женщин в возрасте 40–49 лет среди причин смерти РШМ занимает 2-е место (15,7 %) после РМЖ (22,6 %), в возрастной когорте 50–59 лет – 3-е место (7,5 %) после РМЖ (20,3 %) и рака яичников (8,4 %). Однако в возрастной группе 30–39 лет РШМ является основной причиной смерти (21,3 %), опережая РМЖ (19,6 %) и опухоли лимфатической и кроветворной тканей (9,9 %). В целом наибольший удельный вес смертности от РШМ выявлен у женщин репродуктивного возраста – до 35 лет и 35–44 лет: 44,23 и 39,26 % соответственно [23, 24].
Почему так важен скрининг?
Анализ статистических данных отражает тот факт, что в настоящее время РШМ имеет тенденцию к омоложению, затрагивая наиболее социально значимый контингент населения [24, 30–35]. Учитывая рост населения, а также увеличение продолжительности жизни, статистически прогнозируется, что абсолютное число случаев заболевания и смерти будет расти во всем мире в ближайшие десятилетия (ВОЗ, 2020 г.). Данный прогноз отображен на рис. 5.
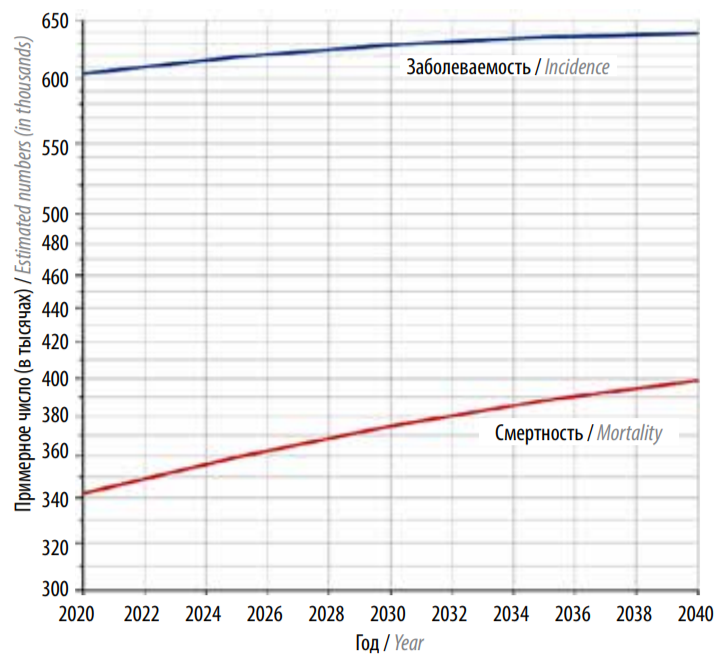
Рис. 5. Прогнозирование заболеваемости раком шейки матки и смертности от него в 2020–2040 гг. по данным Всемирной организации здравоохранения [9]
Согласно этому прогнозу, при отсутствии активных профилактических действий к 2040 г. показатели заболеваемости и смертности увеличатся на 32,1 и 40,6 % соответственно (рис. 6, 7) [5, 6, 9, 36–38].

Рис. 6. Прогнозирование заболеваемости раком шейки матки в 2020–2040 гг. по данным Всемирной организации здравоохранения [9]

Рис. 7. Прогнозирование смертности от рака шейки матки в 2020–2040 гг. по данным Всемирной организации здравоохранения [9]
В связи с этим в ряде стран проводятся скрининговые исследования, направленные на своевременное выявление РШМ, поскольку данное заболевание полностью соответствует требованиям популяционного скрининга [36–41] согласно критериям ВОЗ:
- длительный период предрака с возможностью ранней диагностики;
- существуют общепринятые стратегии лечения;
- имеются эффективные методы лечения;
- достаточно чувствительные и специфичные тесты;
- затраты на скрининг экономически оправданы.
Различный социально-экономический статус стран мирового сообщества обусловливает существующие расхождения в установленных ВОЗ скрининговых программах диагностики и лечения рака, что создает огромные проблемы для снижения заболеваемости и повышения эффективности лечебных подходов при РШМ.
Взаимосвязь с другими заболеваниями
Считается надежно установленной тесная корреляционная связь между инфицированием вирусом папилломы человека и риском развития РШМ. Однако в настоящее время только 20–30 % стран внедрили вакцинацию против вируса папилломы человека, поэтому благотворное влияние вакцинации на уровень заболеваемости РШМ и смертности от него, которое уже очевидно в некоторых странах с высоким уровнем дохода, маловероятно в ближайшие несколько десятилетий для большинства стран [39–47].
Кроме того, предполагается, что пандемия COVID-19 оказала существенное влияние на показатели заболеваемости и смертности от онкологических заболеваний в 2020 г., однако этот вопрос на данный момент не отражен в мировой статистике [48–50]. Снижение показателя заболеваемости РШМ в 2020 г. по сравнению с 2019 г. в значительной мере может быть обусловлено неблагоприятным влиянием пандемии COVID-19.
В этот период онкологические службы России и всего мира работали в сложных условиях, были ограничены возможности использования скрининговых программ по выявлению онкопатологии, приостановлено проведение мероприятий по диспансеризации определенных групп взрослого населения. Это, вероятно, и обусловило тенденцию к некоторому снижению зарегистрированных показателей, отражающих заболеваемость злокачественными новообразованиями [23, 24, 48, 49]. Справедливость такого предположения будет установлена в ближайшие годы на фоне снижения «ковидной» нагрузки на медицинские службы.
Таким образом, обобщение приведенной выше информации позволяет прийти к заключению, что повышение эффективности профилактики и лечения РШМ остается актуальной проблемой во всем мире, несмотря на существенные географические и социально-экономические расхождения заболеваемости и четкий градиент роста негативных показателей в странах с более низким уровнем экономического развития. Наряду с повышением доступности и эффективности лечебных пособий организованные программы скрининга в сочетании с расширенным охватом вакцинацией против вируса папилломы человека будут иметь ключевое значение для снижения заболеваемости РШМ и смертности от него в ближайшие десятилетия.

1. Zhang S., Xu H., Zhang L., Qiao Y. Cervical cancer: epidemiology, risk factors and screening. Chin J Cancer Res 2020;32(6):720–28. DOI: 10.21147/j.issn.1000-9604.2020.06.05
2. Choi S., Ismail A., Pappas-Gogos G., Boussios S. HPV and cervical cancer: a review of epidemiology and screening uptake in the UK. Pathogens 2023;12:298. DOI: 10.3390/pathogens12020298
3. Nygård M., Nygård S. The future of cervical cancer prevention: from “one-size-fits-all” to personalized screening. J Pers Med 2023;13:161. DOI: 10.3390/jpm13020161
4. Gopu P., Antony F., Cyriac S. et al. Updates on systemic therapy for cervical cancer. Ind J Med Res 2021;154(2):293–302. DOI: 10.4103/ijmr.IJMR_4454_20
5. Bray F., Ferlay J., Soerjomataram I. et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018;68(6): 394–424. DOI: 10.3322/caac.21492
6. Sung H., Ferlay J., Siegel R.L. et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021;71(3):209–49. DOI: 10.3322/caac.21660
7. Arbyn M., Weiderpass E., Bruni L. et al. Estimates of incidence and mortality of cervical cancer in 2018: a worldwide analysis. Lancet Glob Health 2020;8(2):191–203. DOI: 10.1016/s2214-109X(19)30482-6
8. Fowler J.R., Maani E.V., Dunton C.J., Jack B.W. Cervical Cancer. 2022. Treasure Island: StatPearls Publishing, 2022. Available at: https://www.ncbi.nlm.nih.gov/books/NBK431093/.
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
5. Bray F., Ferlay J., Soerjomataram I. et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018;68(6): 394–424. DOI: 10.3322/caac.21492
6. Sung H., Ferlay J., Siegel R.L. et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021;71(3):209–49. DOI: 10.3322/caac.21660
7. Arbyn M., Weiderpass E., Bruni L. et al. Estimates of incidence and mortality of cervical cancer in 2018: a worldwide analysis. Lancet Glob Health 2020;8(2):191–203. DOI: 10.1016/s2214-109X(19)30482-6
8. Fowler J.R., Maani E.V., Dunton C.J., Jack B.W. Cervical Cancer. 2022. Treasure Island: StatPearls Publishing, 2022. Available at: https://www.ncbi.nlm.nih.gov/books/NBK431093/.
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
10. Ferlay J., Ervik M., Lam F. et al. Global Cancer Observatory: Cancer Today. International Agency for Research on Cancer. Available at: https://gco.iarc.fr/today.
11. Siegel R.L., Miller K.D., Jemal A. Cancer statistics, 2019. CA Cancer J Clin 2019;69(1):7–34. DOI: 10.3322/caac.21551 12. Shrestha A.D., Neupane D., Vedsted P., Kallestrup P. Cervical cancer prevalence, incidence and mortality in low and middle income countries: a systematic review. Asian Pac J Cancer Prev 2018;19(2):319–24. DOI: 10.22034/APJCP.2018.19.2.319
8. Fowler J.R., Maani E.V., Dunton C.J., Jack B.W. Cervical Cancer. 2022. Treasure Island: StatPearls Publishing, 2022. Available at: https://www.ncbi.nlm.nih.gov/books/NBK431093/.
12. Shrestha A.D., Neupane D., Vedsted P., Kallestrup P. Cervical cancer prevalence, incidence and mortality in low and middle income countries: a systematic review. Asian Pac J Cancer Prev 2018;19(2):319–24. DOI: 10.22034/APJCP.2018.19.2.319
13. Lemp J.M., De Neve J.W., Bussmann H. et al. Lifetime prevalence of cervical cancer screening in 55 low- and middle-income countries. JAMA 2020;324(15):1532–42. DOI: 10.1001/jama.2020.16244
14. Singh G.K., Azuine R.E., Siahpush M. Global inequalities in cervical cancer incidence and mortality are linked to deprivation, low socioeconomic status, and human development. Int J Mch Aids 2012;1(1):17–30. DOI: 10.21106/ijma.12
5. Bray F., Ferlay J., Soerjomataram I. et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018;68(6): 394–424. DOI: 10.3322/caac.21492
12. Shrestha A.D., Neupane D., Vedsted P., Kallestrup P. Cervical cancer prevalence, incidence and mortality in low and middle income countries: a systematic review. Asian Pac J Cancer Prev 2018;19(2):319–24. DOI: 10.22034/APJCP.2018.19.2.319
13. Lemp J.M., De Neve J.W., Bussmann H. et al. Lifetime prevalence of cervical cancer screening in 55 low- and middle-income countries. JAMA 2020;324(15):1532–42. DOI: 10.1001/jama.2020.16244
14. Singh G.K., Azuine R.E., Siahpush M. Global inequalities in cervical cancer incidence and mortality are linked to deprivation, low socioeconomic status, and human development. Int J Mch Aids 2012;1(1):17–30. DOI: 10.21106/ijma.12
13. Lemp J.M., De Neve J.W., Bussmann H. et al. Lifetime prevalence of cervical cancer screening in 55 low- and middle-income countries. JAMA 2020;324(15):1532–42. DOI: 10.1001/jama.2020.16244
14. Singh G.K., Azuine R.E., Siahpush M. Global inequalities in cervical cancer incidence and mortality are linked to deprivation, low socioeconomic status, and human development. Int J Mch Aids 2012;1(1):17–30. DOI: 10.21106/ijma.12
15. Broberg G., Wang J., Östberg A.L. et al. Socio-economic and demographic determinants affecting participation in the Swedish cervical screening program: a population-based case-control study. PLoS One 2018;13(1):e0190171. DOI: 10.1371/journal.pone.0190171
16. Endale H., Mulugeta T., Habte T. The socioeconomic impact of cervical cancer on patients in ethiopia: evidence from Tikur Anbessa Specialized Hospital. Cancer Manag Res 2022;14:1615–25. DOI:10.2147/CMAR.S352389
17. Akinyemiju T., Ogunsina K., Sakhuja S. Life-course socioeconomic status and breast and cervical cancer screening: analysis of the WHO’s Study on Global Ageing and Adult Health (SAGE). BMJ Open 2016;6:012753. DOI: 10.1136/bmjopen-2016-012753
18. Xu T., Yang X., He X. The study on cervical cancer burden in 127 countries and its socioeconomic influence factors. J Epidemiol Glob Health 2023;13:154–61. DOI: 10.1007/s44197-022-00081-1
19. Hull R., Mbele M., Makhafola T. et al. Cervical cancer in low and middleincome countries (review). Oncol Lett 2020;20:2058–74.
5. Bray F., Ferlay J., Soerjomataram I. et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018;68(6): 394–424. DOI: 10.3322/caac.21492
6. Sung H., Ferlay J., Siegel R.L. et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021;71(3):209–49. DOI: 10.3322/caac.21660
11. Siegel R.L., Miller K.D., Jemal A. Cancer statistics, 2019. CA Cancer J Clin 2019;69(1):7–34. DOI: 10.3322/caac.21551
19. Hull R., Mbele M., Makhafola T. et al. Cervical cancer in low and middleincome countries (review). Oncol Lett 2020;20:2058–74.
20. Bhatla N., Berek J.S., CuelloFredes M. et al. Revised FIGO staging for carcinoma of the cervix uteri. Int J Gynaecol Obstet 2019;145(1):129–35. DOI: 10.1002/ijgo.12749
21. Koh W.J., Abu-Rustum N.R., Bean S. et al. Cervical Cancer, Version 3.2019, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw 2019;17(1):64–84. DOI: 10.6004/jnccn.2019.0001
22. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 250 с. Malignant neoplasms in Russia in 2019 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2020. 250 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
22. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 250 с. Malignant neoplasms in Russia in 2019 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the
National Medical Research Radiology Center, Ministry of Health of Russia, 2020. 250 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
22. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 250 с. Malignant neoplasms in Russia in 2019 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the
National Medical Research Radiology Center, Ministry of Health of Russia, 2020. 250 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
25. Крикунова Л.И. Лучевая терапия рака шейки матки. Практическая онкология 2002;3(3):194–9. Krikunova L.I. Radiation therapy for cervical cancer. Prakticheskaya onkologiya = Practical Oncology 2002;3(3):194–9. (In Russ.)
26. Бохман Я.В. Руководство по онкогинекологии. Л.: Медицина, 1989. C. 164–72. Bohman Ya.V. Guide to oncogynecology. Leningrad: Meditsina, 1989. Pp. 164–172. (In Russ.)
27. Полякова В.А. Онкогинекология. Руководство для врачей. M.: Медицинская книга, 2001. 152 с. Polyakova V.A. Oncogynecology. Guide for doctors. Moscow: Meditsinskaya kniga, 2001. 152 p. (In Russ.)
28. Леонов М.Г., Шелякина Т.В., Лукьянова Л.В., Чернов С.Н. Исторические аспекты цитологического скрининга рака шейки матки. Волгоградский научно-медицинский журнал 2012;36(4):6–11. Leonov M.G., Shelyakina T.V., Lukyanova L.V., Chernov S.N. Historical aspects of cytological screening for cervical cancer. Volgogradskiy nauchno-medicinskiy zhurnal = Volgograd Medical Scientific Journal 2012;36(4):6–11. (In Russ.)
29. Мкртчян Л.С., Каприн А.Д., Иванов С.А. и др. Эффективность лечения местнораспространенного рака шейки матки в зависимости от факторов прогноза. Вопросы онкологии 2019;65(4):584–9. Mkrtchyan L.S., Kaprin A.D., Ivanov S.A. et al. Efficiency of treatment of locally advanced cervical cancer depending on prognostic factors. Voprosy onkologii = Oncology Issues 2019;65(4):584–9. (In Russ.)
30. Мкртчян Л.С. Химиолучевое лечение местнораспространенного рака шейки матки и факторы прогноза. Автореф. диc. … д-ра мед. наук. Обнинск, 2019. 328 с. Mkrtchyan L.S. Chemoradiation treatment of locally advanced cervical cancer and prognostic factors. Thesis … doctor of medical sciences. Obninsk, 2019. 328 p. (In Russ.)
31. Хохлова С.В., Коломиец Л.А., Кравец О.А. и др. Практические рекомендации по лекарственному лечению рака шейки матки. Злокачественные опухоли: практические рекомендации RUSSCO 2018;8(3s2):178–89. Доступно по: https://www.rosoncoweb.ru/standarts/RUSSCO/2018/2018-12.pdf. Khokhlova S.V., Kolomiets L.A., Kravets O.A. et al. Practical guidelines for the drug treatment of cervical cancer. Zlokachestvennye opukholi: prakticheskie rekomendatsii RUSSCO = Malignant tumors: practice guidelines RUSSCO 2018;8(3s2):178–89. Available at: https://www.rosoncoweb.ru/ standards/RUSSCO/2018/2018-12.pdf. (In Russ.)
32. Хохлова С.В., Коломиец Л.А., Кравец О.А. и др. Практические рекомендации по лекарственному лечению рака шейки матки. Злокачественные опухоли: практические рекомендации RUSSCO 2020;10(3s2):221–41. Доступно по: https://rosoncoweb.ru/standarts/RUSSCO/2020/2020-13.pdf. Khokhlova S.V., Kolomiets L.A., Kravets O.A. et al. Practical recommendations for the drug treatment of cancer of the cervix. Zlokachestvennye opukholi: prakticheskie rekomendatsii RUSSCO = Malignant tumors: practice guidelines RUSSCO 2020;10(3s2):221–41. Available at: https://rosoncoweb.ru/ standards/RUSSCO/2020/2020-13.pdf. (In Russ.)
33. Рак шейки матки. Клинические рекомендации Ассоциации онкологов России. М.: Минздрав России, 2019. 66 c. Cervical Cancer. Clinical recommendations of the Association of Oncologists of Russia. Moscow: Ministry of Health of Russia, 2019. 66 p. (In Russ.)
34. Каприн А.Д., Мардынский Ю.С. Терапевтическая радиология. Национальное руководство. М.: ГЭОТАР-Медиа, 2018. 704 с. Kaprin A.D., Mardynskiy Yu.S. Therapeutic radiology. National leadership. Moscow: GEOTAR-Media, 2018. 704 p. (In Russ.)
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
30. Мкртчян Л.С. Химиолучевое лечение местнораспространенного рака шейки матки и факторы прогноза. Автореф. диc. … д-ра мед. наук. Обнинск, 2019. 328 с. Mkrtchyan L.S. Chemoradiation treatment of locally advanced cervical cancer and prognostic factors. Thesis … doctor of medical sciences. Obninsk, 2019. 328 p. (In Russ.)
31. Хохлова С.В., Коломиец Л.А., Кравец О.А. и др. Практические рекомендации по лекарственному лечению рака шейки матки. Злокачественные опухоли: практические рекомендации RUSSCO 2018;8(3s2):178–89. Доступно по: https://www.rosoncoweb.ru/standarts/RUSSCO/2018/2018-12.pdf. Khokhlova S.V., Kolomiets L.A., Kravets O.A. et al. Practical guidelines for the drug treatment of cervical cancer. Zlokachestvennye opukholi: prakticheskie rekomendatsii RUSSCO = Malignant tumors: practice guidelines RUSSCO
2018;8(3s2):178–89. Available at: https://www.rosoncoweb.ru/ standards/RUSSCO/2018/2018-12.pdf. (In Russ.)
32. Хохлова С.В., Коломиец Л.А., Кравец О.А. и др. Практические рекомендации по лекарственному лечению рака шейки матки. Злокачественные опухоли: практические рекомендации RUSSCO 2020;10(3s2):221–41. Доступно по: https://rosoncoweb.ru/standarts/RUSSCO/2020/2020-13.pdf. Khokhlova S.V., Kolomiets L.A., Kravets O.A. et al. Practical recommendations for the drug treatment of cancer of the cervix. Zlokachestvennye opukholi: prakticheskie rekomendatsii RUSSCO = Malignant tumors: practice guidelines RUSSCO 2020;10(3s2):221–41. Available at: https://rosoncoweb.ru/ standards/RUSSCO/2020/2020-13.pdf. (In Russ.)
33. Рак шейки матки. Клинические рекомендации Ассоциации онкологов России. М.: Минздрав России, 2019. 66 c. Cervical Cancer. Clinical recommendations of the Association of Oncologists of Russia. Moscow: Ministry of Health of Russia, 2019. 66 p. (In Russ.)
34. Каприн А.Д., Мардынский Ю.С. Терапевтическая радиология. Национальное руководство. М.: ГЭОТАР-Медиа, 2018. 704 с. Kaprin A.D., Mardynskiy Yu.S. Therapeutic radiology. National leadership. Moscow: GEOTAR-Media, 2018. 704 p. (In Russ.)
35. Хохлова С.В., Деньгина Н.В., Коломиец Л.А. и др. Практические рекомендации по лекарственному лечению рака шейки матки. Злокачественные опухоли: практические рекомендации RUSSCO 2017;7(3s2):158–67. Доступно по: https://www.rosoncoweb.ru/standarts/RUSSCO/2017/recoms2017_11.pdf. Khokhlova S.V., Dengina N.V., Kolomiets L.A. et al. Practical recommendations for the drug treatment of cancer of the cervix. Zlokachestvennye opukholi: prakticheskie rekomendatsii RUSSCO = Malignant tumors: practice guidelines RUSSCO 2017;7(3s2):158–67. Available at: https://www.rosoncoweb.ru/standards/RUSSCO/2017/recoms2017_11.pdf. (In Russ.)
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
5. Bray F., Ferlay J., Soerjomataram I. et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2018;68(6): 394–424. DOI: 10.3322/caac.21492
6. Sung H., Ferlay J., Siegel R.L. et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin 2021;71(3):209–49. DOI: 10.3322/caac.21660
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
36. World Health Organization (WHO). WHO Director-General calls for all countries to take action to help end the suffering caused by cervical cancer. Geneva: World Health Organization, 2018. Available at: https://www.who.int/news/item/18-05-2018-who-dg-calls-for-all-countries-to-take-action-to-help-end-the-suffering-caused-by-cervical-cancer.
37. World Health Organization (WHO). Global Strategy to Accelerate the Elimination of Cervical Cancer as a Public Health Problem. Geneva: World Health Organization, 2020.
38. WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, second edition. Geneva: World Health Organization, 2021.
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
9. Singh D., Vignat J., Lorenzoni V. et al. Global estimates of incidence and mortality of cervical cancer in 2020: a baseline analysis of the WHO Global Cervical Cancer Elimination Initiative. Lancet Glob Health 2023;11(2):197–206. DOI: 10.1016/S2214-109X(22)00501-0
36. World Health Organization (WHO). WHO Director-General calls for all countries to take action to help end the suffering caused by cervical cancer. Geneva: World Health Organization, 2018. Available at: https://www.who.int/news/item/18-05-2018-who-dg-calls-for-all-countries-to-take-action-to-help-end-the-suffering-caused-by-cervical-cancer.
37. World Health Organization (WHO). Global Strategy to Accelerate the Elimination of Cervical Cancer as a Public Health Problem. Geneva: World Health Organization, 2020.
38. WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, second edition. Geneva: World Health Organization, 2021.
39. Brisson M., Kim J.J., Canfell K. et al. Impact of HPV vaccination and cervical screening on cervical cancer elimination: a comparative modelling analysis in 78 low-income and lower-middle-income countries. Lancet 2020;395(10224):575–90. DOI: 10.1016/S0140-6736(20)30068-4
40. Canfell K., Kim J.J., Brisson M. et al. Mortality impact of achieving WHO cervical cancer elimination targets: a comparative modelling analysis in 78 low-income and lower-middle-income countries. Lancet 2020;395(10224):591–603. DOI: 10.1016/S0140-6736(20)30157-4.
41. Bruni L., Saura-Lázaro A., Montoliu A. et al. HPV vaccination introduction worldwide and WHO and UNICEF estimates of national HPV immunization coverage 2010–2019. Prev Med 2021;144(106399):1–11. DOI: 10.1016/j.ypmed.2020.106399
39. Brisson M., Kim J.J., Canfell K. et al. Impact of HPV vaccination and cervical screening on cervical cancer elimination: a comparative modelling analysis in 78 low-income and lower-middle-income countries. Lancet 2020;395(10224):575–90. DOI: 10.1016/S0140-6736(20)30068-4
40. Canfell K., Kim J.J., Brisson M. et al. Mortality impact of achieving WHO cervical cancer elimination targets: a comparative modelling analysis in 78 low-income and lower-middle-income countries. Lancet 2020;395(10224):591–603. DOI: 10.1016/S0140-6736(20)30157-4.
41. Bruni L., Saura-Lázaro A., Montoliu A. et al. HPV vaccination introduction worldwide and WHO and UNICEF estimates of national HPV immunization coverage 2010–2019. Prev Med 2021;144(106399):1–11. DOI: 10.1016/j.ypmed.2020.106399
42. Briolat J., Dalstein V., Saunier M. et al. HPV prevalence, viral load and physical state of HPV-16 in cervical smears of patients with different grades of CIN. Int J Cancer 2007;121(10):2198–204. DOI: 10.1002/ijc.22959
43. Шипулина О.Ю. Эпидемиологические особенности и меры профилактики онкогинекологической патологии папиллома-вирусной этиологии. Автореф. дис. … канд. мед. наук. М., 2013. 24 с. Shipulina O.Yu. Epidemiological features and measures for the prevention of oncogynecological pathology of papillomavirus etiology. Thesis … candidate of medical sciences. Moscow, 2013. 24 p. (In Russ.)
44. Протасова А.Э. Цервикальная интраэпителиальная неоплазия и рак шейки матки. Вирус папилломы человека – единственный фактор риска? Эффективная фармакотерапия 2019;15(32):42–6. DOI: 10.33978/2307-3586-2019-15-32-42-46 Protasova A.E. Cervical intraepithelial neoplasia and cervical cancer. Is human papillomavirus the only risk factor? Effektivnaya farmakoterapiya = Effective pharmacotherapy 2019;15(32):42–6. (In Russ.). DOI: 10.33978/2307-3586-2019-15-32-42-46
45. ARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Human Papillomaviruses. Lyon, 2007. 636 p.
46. Walboomers J.M., Jacobs M.V., Manos M.M. et al. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J Pathol 1999;189(1):12–9. DOI: 10.1002/(SICI)10969896(199909)189:1<12::AID-PATH431>3.0.CO;2-F
47. Bruni L., Albero G., Serrano B. et al. ICO/IARC Information Centre on HPV and Cancer (HPV Information Centre). Human Papillomavirus and Related Diseases in the World, 2021. 314 p.
48. Ashamalla H., Ashamalla M., McFarlane S.I. COVID-19 pandemic and the new state of oncology practice: an editorial. Am J Med Case Rep 2020;8(9):311, 312. DOI: 10.12691/ajmcr-8-9-13
49. Maringe C., Spicer J., Morris M. et al. The impact of the COVID-19 pandemic on cancer deaths due to delays in diagnosis in England, UK: a national, population-based, modelling study. Lancet Oncol 2020;21(8):1023–34. DOI: 10.1016/S1470-2045(20)30388-0
50. Chino J., Annunziata C.M., Beriwal S. et al. The ASTRO clinical practice guidelines in cervical cancer: optimizing radiation therapy for improved outcomes. Gynecol Oncol 2020;159(3):607–10. DOI: 10.1016/j.ygyno.2020.09.015
23. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant neoplasms in Russia in 2020 (morbidity and mortality). Eds.: A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. M.: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
24. Состояние онкологической помощи населению России в 2021 г. Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 239 с. The state of oncological care for the population of Russia in 2021, Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 239 p. (In Russ.)
48. Ashamalla H., Ashamalla M., McFarlane S.I. COVID-19 pandemic and the new state of oncology practice: an editorial. Am J Med Case Rep 2020;8(9):311, 312. DOI: 10.12691/ajmcr-8-9-13
49. Maringe C., Spicer J., Morris M. et al. The impact of the COVID-19 pandemic on cancer deaths due to delays in diagnosis in England, UK: a national, population-based, modelling study. Lancet Oncol 2020;21(8):1023–34. DOI: 10.1016/S1470-2045(20)30388-0



















