
Введение
В настоящее время вопросы вторичной профилактики РШМ сохраняют свою актуальность. В период пандемии новой коронавирусной инфекции наметилась тенденция к снижению первичной заболеваемости и смертности вследствие РШМ. Однако сохраняется значительная доля случаев выявления запущенных стадий рака данной визуальной локализации и уменьшился удельный вес активного выявления опухоли [1]. В допандемийный период, в 2019 году, первичная заболеваемость РШМ («грубый» показатель) в Российской Федерации составила 22,25 на 100 тыс. женщин. Смертность зарегистрирована на уровне 8,12 («грубый» показатель) на 100 тыс. женщин. Из всех пациенток с онкологическими заболеваниями органов женской репродуктивной системы пациентки с РШМ имели наименьший возраст [1]. По данным медицинских организаций г. Екатеринбурга, «грубый» показатель первичной заболеваемости РШМ в 2019 году – 14,20/0000. Смертность от РШМ в 2019 году не превышала 5,80/0000 («грубый» показатель).
Развитие РШМ связывают с длительной персистенцией вируса папилломы человека (ВПЧ) онкогенных генотипов в эпителии шейки матки. Опухоли предшествует цервикальная интраэпителиальная неоплазия (CIN), которая также ассоциирована с влиянием ВПЧ. CIN II и III степени рассматривается как предраковое заболевание шейки матки [2, 3].
Всемирной организацией здравоохранения определена глобальная стратегия комплексного и мультидисциплинарного подхода борьбы с РШМ, которая наряду с первичной профилактикой, включающей вакцинацию от папилломавирусной инфекции прежде всего девочек и мальчиков, предусматривает мероприятия по вторичной профилактике – скринингу на предраковые заболевания шейки матки и их лечению [4]. С 2021 года в Российской Федерации скрининг на предраковые и злокачественные заболевания шейки матки регламентирован Порядком оказания медицинской помощи по профилю «акушерство и гинекология» и Порядком проведения профилактического медицинского осмотра и диспансеризации определенных групп населения, клиническими рекомендациями [5, 6]. Кроме того, лечение CIN не всегда бывает успешным, возможны рецидивы [7]. В связи с этим актуальной является аналитическая информация о заболеваемости предраком – CIN – для принятия организационных решений, планирования лечебно-диагностических мероприятий и контроля эффективности медицинской помощи.
Материалы и методы
Проведено описательное эпидемиологическое исследование заболеваемости CIN и доброкачественными заболеваниями шейки матки (ЭЭ, лейкоплакией, полипом эндоцервикса) в популяции женщин г. Екатеринбурга. Для анализа использовали сведения женских консультаций медицинских организаций города о численности заболевших женщин в возрасте 18 лет и старше в 2013–2019 годах. Исследовали форму Федерального статистического наблюдения №12 «Сведения о числе заболеваний, зарегистрированных у пациентов, проживающих в районе обслуживания медицинской организации» (ФСН №12) в части ЭЭ и данные женских консультаций города о числе женщин, заболевших CIN, лейкоплакией и полипом шейки матки, по обращаемости. Диагностика заболеваний включала клиническое, цитологическое, кольпоскопическое и патоморфологическое обследования. Постановка диагноза и учет заболеваний соответствовали установленным требованиям [2, 3].
Показатели первичной и общей заболеваемости рассчитывали на 100 тыс. женского населения в возрасте 18 лет и старше за календарный год (отчетный период) по формулам, рекомендованным Федеральной службой государственной статистики, ФГБУ «Центральный научно-исследовательский институт организации и информатизации здравоохранения» Минздрава России, и выражали в 0/0000 [8, 9]. При расчете показателя использовали сведения о численности женского населения г. Екатеринбурга в 2013–2019 годах, предоставленные Управлением Федеральной службы государственной статистики по Свердловской и Курганской областям. Для описания динамики цервикальной патологии анализировали показатели первичной и общей заболеваемости в 2013–2019 годах, средний уровень заболеваемости по периодам 2013–2016 и 2017–2019 годов, а также относительный прирост показателей заболеваемости по вышеуказанным интервалам наблюдения [10]. Критерием разделения на периоды наблюдения (2013–2016 и 2017–2019 годы) явился год внедрения клинических рекомендаций по патологии шейки матки [2] и реорганизации диагностической службы медицинских учреждений здравоохранения города для цитологических исследований. В нашей работе период наблюдения ограничен годом начала пандемии новой коронавирусной инфекции COVID-19 на территории Российской Федерации. Смена приоритетов и мобилизация системы здравоохранения для оказания медицинской помощи больным с новой коронавирусной инфекцией нашли отражение в снижении показателей заболеваемости населения болезнями неинфекционного профиля, что, вероятно, не отражает истинной картины распространения большинства болезней во время пандемии [11, 12]. Поэтому аналитическая информация о заболеваемости цервикальной патологией в допандемийный период сохраняет свою актуальность, отражает уровень здоровья женского населения во 2-м десятилетии XXI века, является основанием для оценки деятельности акушерско-гинекологической службы и планирования медицинской помощи в будущем.
Статистический анализ проводили с помощью программ Microsoft Excel 2016 и SPSS 23.0 (IBM, США). Показатели первичной заболеваемости сравнивали с помощью Т-критерия для независимых переменных с учетом поправки Даннета на множественные сравнения. Показатели общей заболеваемости исследовали с помощью парного Т-критерия для связных выборок с учетом поправки Бонферрони на множественные сравнения. Различия считали статистически значимыми при р < 0,05.
Результаты
Проведенный анализ показал, что первичная заболеваемость цервикальной эпителиальной неоплазией в 2013 году составляла 66,90/0000 и в течение всего периода наблюдения последовательно увеличивалась (рис. 1). В 2014–2015 годах изменения имели характер тенденции. С 2016 года наблюдался статистически значимый рост первичной заболеваемости в 1,7 раза по сравнению с 2013 годом (р < 0,001). В 2017 году (р < 0,001) и 2018 году (р < 0,001) увеличение показателя продолжилось и достигло максимального значения в 2019 году – 215,50/0000, превышая первичную заболеваемость CIN в 2013 году в 3,2 раза (р <0,001). При анализе среднего уровня первичной заболеваемости по периодам наблюдения следует отметить, что в 2017–2019 годах показатель увеличился в 2 раза по сравнению с 2013–2016 годами (р < 0,001) (рис. 2). Величина относительного прироста среднего уровня первичной заболеваемости CIN в 2017–2019 годах составила 101,8% и подтвердила вывод о значимом увеличении заболеваемости CIN.
Динамика первичной заболеваемости ЭЭ, лейкоплакией и полипом шейки матки в 2013–2019 годах характеризовалась отсутствием статистически значимых изменений (р > 0,05) (см. рис. 1).
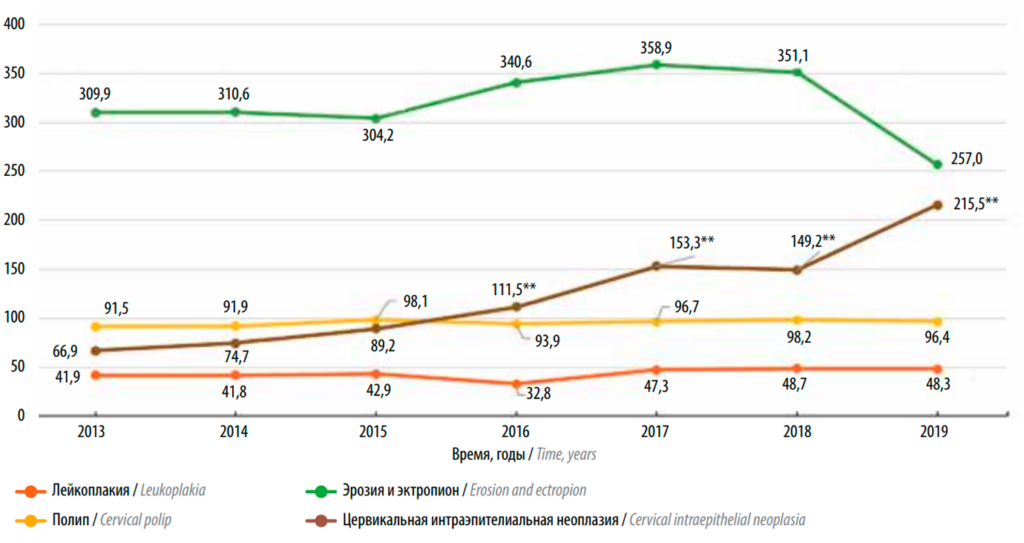
Рис. 1. Первичная заболеваемость цервикальной интраэпителиальной неоплазией, эрозией и эктропионом, лейкоплакией, полипом шейки матки в 2013–2019 годах (на 100 тыс. женского населения в возрасте 18 лет и старше). *p < 0,05; **p < 0,001, сравнение с 2013 года, T-критерий для независимых групп с учетом поправки на множественные сравнения (критерий Даннета)
Аналогичная тенденция наблюдалась для среднего уровня первичной заболеваемости по периодам наблюдения (р > 0,05) (см. рис. 2). Относительный прирост среднего уровня первичной заболеваемости в 2017–2019 годах составил для ЭЭ 1,9%, для полипа эндоцервикса – 2,9%, для лейкоплакии – 10,6%.
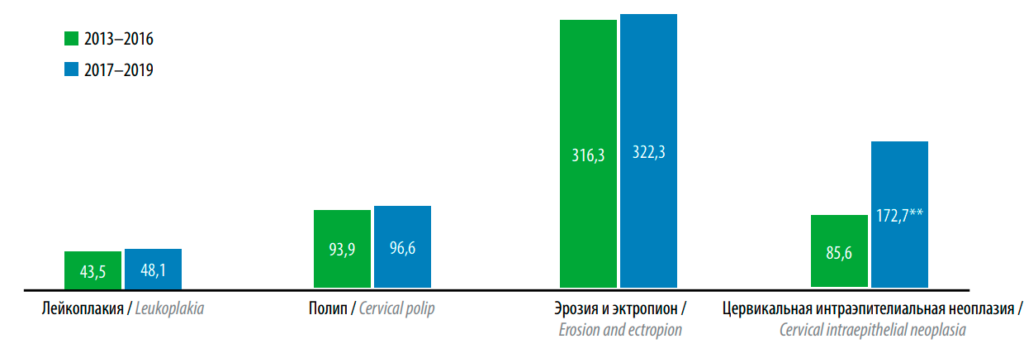
Рис. 2. Средний уровень первичной заболеваемости цервикальной интраэпителиальной неоплазией, эрозией и эктропионом, лейкоплакией, полипом шейки матки в 2013–2016 и 2017–2019 годах (на 100 тыс. женского населения в возрасте 18 лет и старше). *p < 0,05; **p < 0,001, сравнение с 2013–2016 годов, T-критерий для независимых групп с учетом поправки на множественные сравнения (критерий Даннета)
В 2013 году общая заболеваемость СIN составила 144,4 0/0000 и ежегодно увеличивалась за весь период наблюдения. Статистически значимый рост показателя наблюдался с 2014 по 2019 год в сопоставлении с 2013 годом (р < 0,001) (рис. 3). В 2019 году показатель общей заболеваемости СIN был 303,1 0/0000, в 2,1 раза превышая значение в 2013 году (р < 0,001).
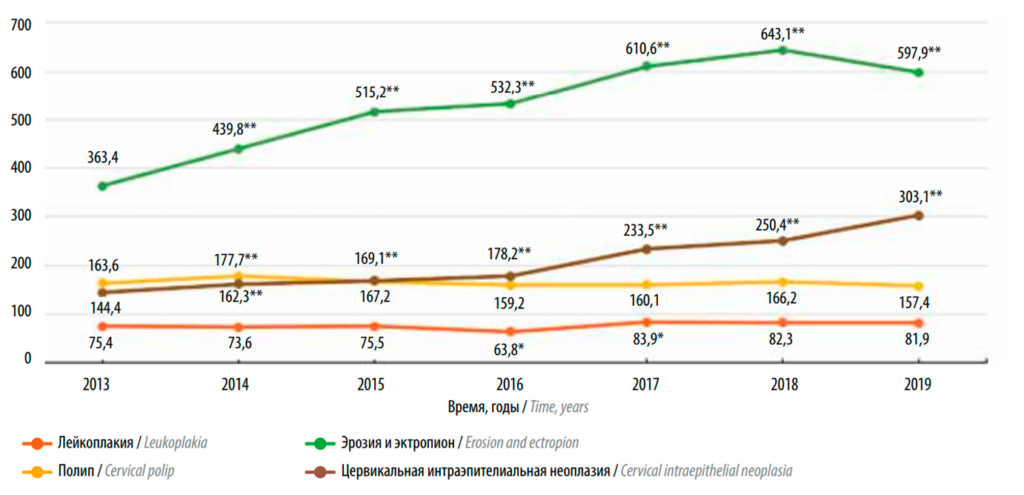
Рис. 3. Общая заболеваемость цервикальной интраэпителиальной неоплазией, эрозией и эктропионом, лейкоплакией, полипом шейки матки в 2013–2019 годах (на 100 тыс. женского населения в возрасте 18 лет и старше). *p < 0,05; **p < 0,001, сравнение с 2013 года, парный T-критерий для связных групп с учетом поправки Бонферрони на множественные сравнения
Общая заболеваемость ЭЭ имела динамику, аналогичную для СIN. Статистически значимый рост показателя наблюдался с 2014 года. Уровень общей заболеваемости ЭЭ в 2019 году составил 597,9 0/0000 и был в 1,6 раза больше, чем в 2013 году (р < 0,001). Средний уровень общей заболеваемости CIN в 2017–2019 годах увеличился в 1,6 раза по сравнению с 2013–2016 годами (р < 0,001) (рис. 4). Увеличение среднего уровня общей заболеваемости ЭЭ было менее интенсивным, чем для CIN. Относительный прирост составил 33,4% и значимо превышал величину в 2013–2016 годах (р < 0,001).
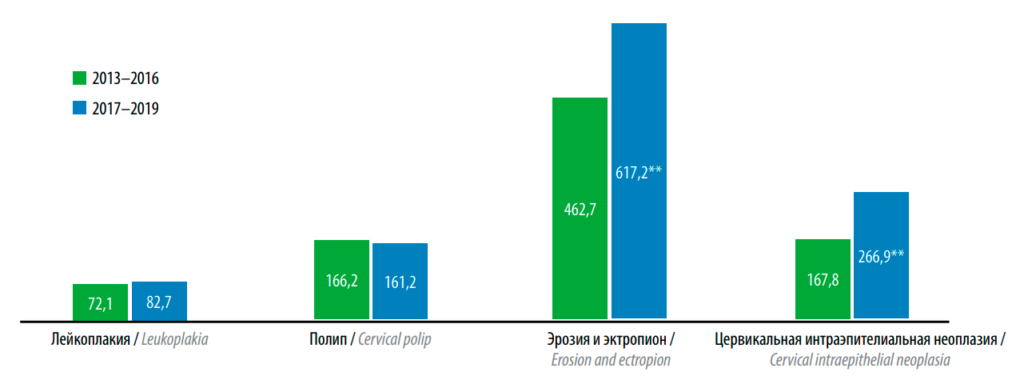
Рис. 4. Средний уровень общей заболеваемости цервикальной интраэпителиальной неоплазией, эрозией и эктропионом, лейкоплакией, полипом шейки матки в 2013–2016 и 2017–2019 годах (на 100 тыс. женского населения в возрасте 18 лет и старше). *p < 0,05; **p < 0,001, сравнение с 2013–2016 годами, парный T-критерий для связных групп с учетом поправки Бонферрони на множественные сравнения
Динамика общей заболеваемости полипом и лейкоплакией шейки матки в наблюдаемый период не имела тенденции к росту (р > 0,05) и характеризовалась стабильностью показателя (см. рис. 3–4). Относительный прирост среднего уровня общей заболеваемости составил для лейкоплакии 14,7%, а для полипа эндоцервикса отмечено отрицательное значение (убыль), равное –3%.
Обсуждение
Уровень заболеваемости CIN различается в популяциях женщин [13, 14, 15]. Ранее, в начале XXI века, в литературе была описана динамика заболеваемости CIN у женщин г. Екатеринбурга. В предшествующий период первичная заболеваемость CIN последовательно увеличивалась, показатель вырос в 2 раза. CIN занимала 2-е место среди заболеваний шейки матки [15]. По результатам наших исследований, в 2013–2019 годах рост первичной заболеваемости CIN продолжился. В 2014, 2015 и 2016 годах ежегодно регистрировался прирост показателя. Лишь в 2016 году и позднее (2017–2019 годы) показатель стал статистически значимой величиной и достиг максимального значения в 2019 году. Полагаем, что рост заболеваемости CIN, с одной стороны, обусловлен естественным распространением заболевания и инфицированием ВПЧ на фоне частичной вакцинации, с другой – выявленную динамику следует рассматривать как положительную тенденцию организации и оказания медицинской помощи по активному выявлению патологии шейки матки на стадии предрака, что позволяет провести своевременное лечение и предотвратить развитие онкологического заболевания. Именно в 2016–2019 годах уделялось большое внимание проведению профилактических осмотров и диспансеризации определенных групп взрослого населения, включающих цитологический скрининг как один из этапов диагностики CIN. Поэтому рост первичной заболеваемости следует связать с обращаемостью пациенток, в частности с увеличением числа женщин, обследованных на онкозаболевания в женских консультациях и смотровых кабинетах в рамках профилактических мероприятий.
Кроме того, большое значение имеет качество диагностики на амбулаторным этапе акушерско-гинекологической службы, что определяется материально-техническим оснащением, уровнем лабораторно-диагностической базы, подготовкой кадров. Данный тезис поясняют некоторые организационные решения и методические шаги, которые были использованы. Методологической основой для технологического обеспечения и последипломной подготовки специалистов амбулаторного звена акушерско-гинекологической службы города явились клинические рекомендации [2], которые позволили сделать акцент на выявлении и лечении предраковых заболеваний, повышении качества цервикального скрининга в женских консультациях и смотровых кабинетах поликлиник. Другим направлением стала реорганизация цитологической службы. Исследования из всех больниц города были сконцентрированы в цитологической лаборатории экспертного уровня. В качестве референс-технологий были внедрены жидкостная цитология и типирование пациентов на 16 онкогенных генотипов ВПЧ для уточнения диагноза и оценки эффективности лечения. Положительный вклад внесла систематическая экспертиза качества цитологических исследований. При лечении и диспансерном наблюдении была реализована стратегия концентрации пациенток с предраковыми заболеваниями шейки матки в 2 специализированных центрах. Эти центры оказывали не только лечебно-диагностическую помощь пациенткам, но и методическую поддержку врачам акушерам-гинекологам кабинетов патологии шейки матки женских консультаций, включая внедрение клинических рекомендаций. С 2008 года последипломная подготовка врачей акушеров-гинекологов проводилась в рамках циклов повышения квалификации «Патология шейки матки, влагалища и вульвы с основами кольпоскопии и широкополосной радиохирургии» кафедры акушерства и гинекологии ФБГОУ ВО «Уральский государственный медицинский университет» Минздрава России. Программа обучения включала не только теоретическую подготовку, но и отработку мануальных навыков. Ежегодно обучение проходили более 50 врачей.
Таким образом, для динамики показателя первичной заболеваемости CIN имел значение комплекс мероприятий по активному выявлению патологии шейки матки, включая доступность медицинской помощи (по обращаемости, профилактические осмотры, диспансеризация взрослого населения), уровень материально-технического оснащения женских консультаций и смотровых кабинетов, лабораторно-диагностической базы, подготовки кадров.
В 2019 году первичная заболеваемость CIN стала конкурировать с заболеваемостью ЭЭ за 1-е место в структуре патологии шейки матки. Показатель ЭЭ уменьшился в 2019 году по сравнению с 2018 годом, что объясняется незначительным увеличением численности женского населения при уменьшении числа заболеваний. В данном случае возможно обсуждать роль изменения тактики ведения женщин с эктопией цилиндрического эпителия лечащим врачом. Эктопия шейки матки, в отличие от ЭЭ, рассматривается как физиологическое состояние и не подлежит регистрации в качестве заболевания [2, 3]. Выявленная динамика показателя соответствует тенденции, наблюдаемой в популяции женщин Российской Федерации [16].
Изменения общей заболеваемости CIN, ЭЭ, лейкоплакией и полипом эндоцервикса соответствовали изменениям первичной заболеваемости и отражали кумулятивный эффект при диспансерном наблюдении пациенток.
Следует отметить, что профессиональное акушерско-гинекологическое сообщество страны занимает активную позицию, открыто обозначает «слабые места» цервикального скрининга, уточняет и предлагает новые решения для повышения его эффективности и своевременной диагностики РШМ и предраковых заболеваний [17, 18]. В этом аспекте сведения о численности женщин, заболевших CIN, являются важной информацией для планирования и организации медицинской помощи. В настоящее время информация о заболевших на амбулаторном этапе по обращаемости содержится в форме ФСН №12, которая является официальным документом отраслевой статистики. Учитывая, что среднетяжелая и тяжелая CIN являются предраковыми заболеваниями, целесообразно рассмотреть вопрос о включении шифра №87 «Дисплазия шейки матки» в данную учетную форму для получения объективной информации о распространенности заболевания на уровне страны, субъекта РФ, территориального образования и медицинской организации. Основанием для внесения изменений в форму ФСН №12 могут являться положения действующей редакции Порядков оказания медицинской помощи по профилю «акушерство и гинекология» и по проведению профилактического осмотра и диспансеризации определенных групп населения.
Выводы
В допандемийный период (2013–2019 годы) в г. Екатеринбурге продолжился рост первичной и общей заболеваемости CIN, отмеченный с начала XXI века. В 2019 году показатель первичной заболеваемости СIN имел максимальное значение, конкурируя с заболеваемостью ЭЭ за 1-е место в структуре заболеваний шейки матки. Рост заболеваемости CIN мы связываем с естественным распространением заболевания в популяции женщин, увеличением доступности и повышением качества оказания медицинской помощи. Для планирования и оценки эффективности медицинской помощи по вторичной профилактике РШМ предлагается организовать учет заболеваемости предраковым заболеванием шейки матки (CIN) на уровне отраслевой статистики.

Comprehensive fight against cervical cancer: a guide to the basics of practice. Geneva, 2018. 440 p. Available at: https://www.euro.who.int/__data/assets/pdf_file/0007/383452/c4gep-rus.pdf.
Леонов С.А., Сон И.М., Савина А.А. Руководство по анализу основных статистических показателей состояния здоровья населения и деятельности медицинских организаций. М., 2015. 53 с.
Роговская С.И., Радзинский В.Е., Узденова С.А. и др. Женпросвет/Онкопатруль: новые социальные инициативы. Всероссийский просветительский проект от профессоров для женщин и врачей. Женское здоровье и репродукция 2019;11–12(42–43):40–7.



















