Материалом исследования являлись справочники МНИОИ им. П. А. Герцена и НМИЦ онкологии им. Н. Н. Петрова, база данных популяционного ракового регистра северо-западного федерального округа, клинические материалы хирургического отделения опухолей молочной железы НМИЦ онкологии им. Н.Н. Петрова. Отобрано более 110 тысяч первичных случаев РМЖ. Обработка данных осуществлялась стандартными методами онкологической статистики, рекомендованными международной ассоциацией раковых регистров (программа Eurocare).
Установлено существенное влияние пандемии коронавирусной инфекции на первичную регистрацию РМЖ в Российской федерации с 2019 по 2020 г. и некоторое ослабление ее воздействия в последующий период. Пандемия нанесла существенное влияние на качество первичного учета больных. Величина индекса достоверности учета отброшена на 5 лет назад, но наметился признак ее улучшения в 2021 г. Показана положительная динамика 1- и 5-летней выживаемости больных РМЖ. Исследовано качество регистрации больных РМЖ по детальной локализационной и гистологической структурам РМЖ. Отмечено существенное снижение летальности больных при исследовании закономерностей динамики погодичной летальности на протяжении 3 периодов наблюдения.
Последние публикации Международного агентства по исследованию рака (МАИР) свидетельствуют о том, что рак молочной железы (РМЖ) – самая распространенная онкологическая патология среди женского населения экономически развитых стран [1]. Наиболее высокие стандартизованные показатели заболеваемости женщин (>1000/0000) зарегистрированы в Бельгии, Германии и Дании, минимальные – в Индии (32,70/0000). В России и Северо-Западном федеральном округе Российской Федерации (СЗФО РФ) этот показатель составляет 50,4 и 50,70/0000 соответственно [1], что позволяет нам экстраполировать расчеты показателей выживаемости больных, пролеченных в СЗФО РФ, на всю Россию.
На рисунке 1 представлено сравнение уровней повозрастных показателей заболеваемости женщин и мужчин РМЖ по 4 странам. Везде закономерности повозрастной распространенности опухолей схожи с наивысшими показателями по США.
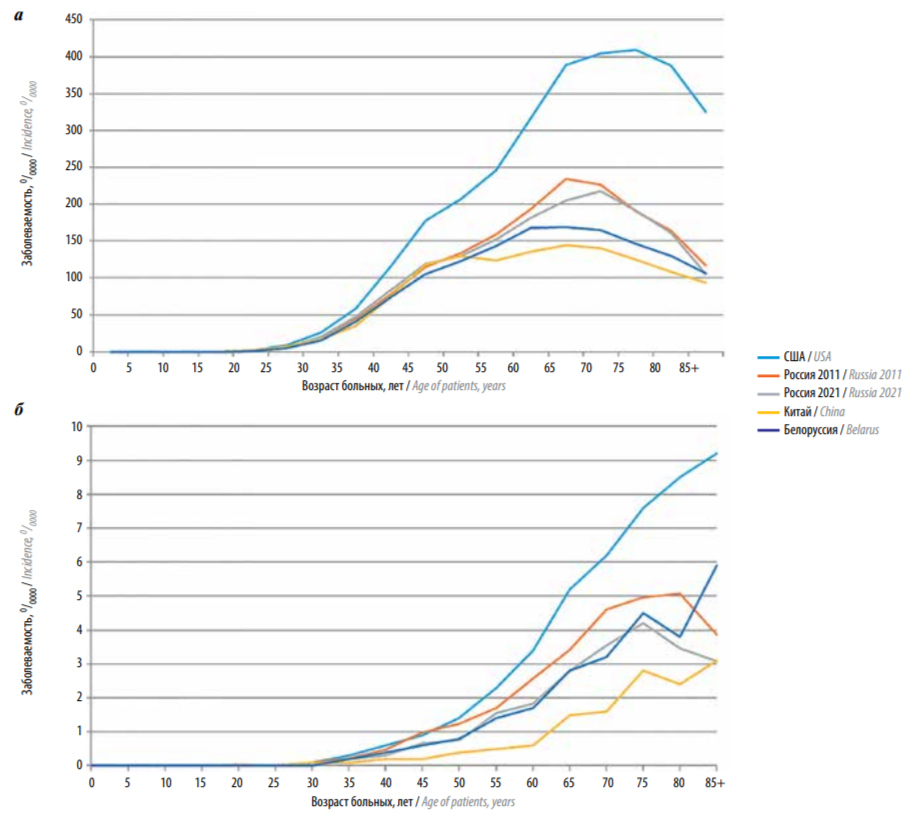
Рис. 1. Повозрастные показатели заболеваемости раком молочной железы женщин (а) и мужчин (б) в некоторых странах [1, 2]
Заболеваемость
В России ежегодно регистрируется >70 тыс. новых случаев РМЖ (70208 в 2021 г.), в том числе учтено 495 случаев среди мужского населения. С 2008 г. абсолютное число новых случаев РМЖ возросло к 2019 г. на 64,8 % (с 44840 до 73918), грубый показатель увеличился с 58,1 до 94,00/0000, или на 61,8 % (оба пола). В 2020 г. в связи с пандемией коронавирусной инфекции в медицинские учреждения не смогли попасть около 8,5 тыс. больных. Динамика стандартизованных показателей заболеваемости женщин РМЖ представлена на рисунке 2.
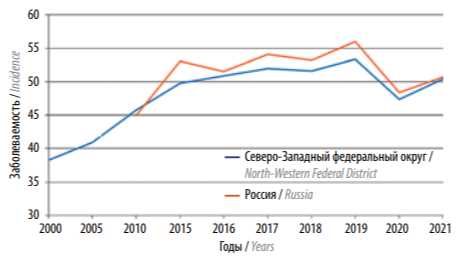
Рис. 2. Стандартизованные показатели заболеваемости женщин раком молочной железы [2–11]
После резкого падения в 2021 г. мы наблюдаем постепенный рост заболеваемости [2–11]. Ранговое распределение уровней стандартизованных показателей заболеваемости женщин РМЖ в России в 2021 г. по административным территориям показало, что наивысшие показатели (>1000/0000) выявлены в Севастополе (116,80/0000), в Ярославской, Тульской, Тверской и Нижегородской областях (115,2; 115,1; 108,0 и 106,90 /0000 соответственно). В г. Санкт-Петербурге этот показатель составил 106,10/0000, в г. Москве – 82,40/0000. Минимальные уровни заболеваемости женщин РМЖ установлены для Республики Дагестан (40,10/0000) и Чукотского автономного округа (28,590/0000). Достоверность учета.
Достоверность учета регулируется индексом достоверности учета, т. е. отношением числа умерших к числу заболевших [12, 13]. В 2000 г. этот показатель в РФ и в СЗФО РФ был >0,4, а к 2019 г. снизился до 0,29, что свидетельствовало о существенном улучшении первичной регистрации больных РМЖ. В 2020 г. пандемия коронавирусной инфекции расстроила налаженную систему раннего выявления больных со злокачественными новообразованиями, были свернуты скрининговые программы, ограничен доступ больных в лечебно-профилактические и специализированные онкологические учреждения, в связи с чем индекс достоверности учета существенно возрос по РФ до 0,33, в СЗФО РФ – до 0,36, что соответствует уровню 2014–2015 гг. (рисунок 3) [2, 6–11].
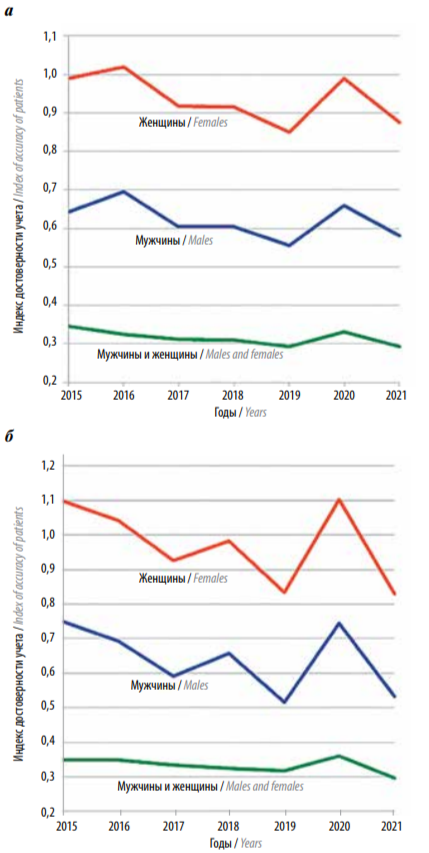
Рис. 3. Индекс достоверности учета больных раком молочной железы в Российской Федерации (а) и в Северо-Западном федеральном округе (б)
Исследование динамики погодичной летальности показало значительное снижение ее показателей за последние 20 лет.
Смертность
В РФ ежегодно погибает >20 тыс. больных РМЖ (20620 в 2021 г.), в том числе 140 мужчин. Стандартизованный показатель смертности женщин от РМЖ с 2000 по 2019 г. снизился с 17,24 до 13,60/0000, или на 21,2 %, а затем, к 2021 г., еще на 6,5 % – до 12,50/0000. На рисунке 4 эти процессы представлены наглядно [2, 6–11]. Особенности локализационной и гистологической структуры больных РМЖ в СЗФО РФ.
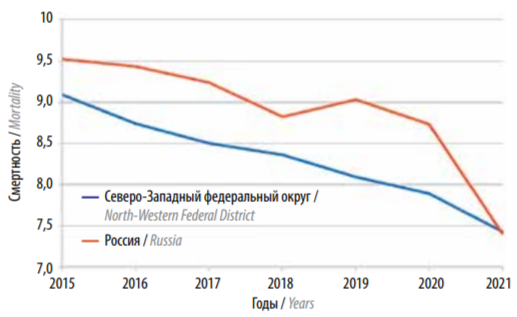
Рис. 4. Динамика смертности населения отрака молочной железы (оба пола)
Особенности динамики детальной локализационной и гистологической структуры изложены нами подробно ранее [12]. По состоянию на 2022 г. они сохранились.
Медиана выживаемости
Медиана – варианта, которая находится в середине вариационного ряда и делит его пополам. Это один из важнейших критериев оценки эффективности противораковой борьбы при расчете показателя выживаемости.
Для локализаций с высоким уровнем летальности медиана выживаемости вычисляется в месяцах; эти данные для рака печени, желудка, легких и некоторых других локализаций мы могли бы получить по состоянию на 2016–2017 гг. Для РМЖ на сегодняшний день сведения о медиане выживаемости возможно получить только по состоянию на 2011 г. Ее величина с 2000 г. находилась в пределах 8–9 лет. Никакого существенного увеличения медианы выживаемости в СЗФО РФ для РМЖ нами не обнаружено. Показатели медианы выживаемости на 2018 г. мы сможем получить не ранее 2028 г. [13, 14].
Наблюдаемая и относительная выживаемость
Расчеты показателей выживаемости на популяционном уровне осуществляются в соответствии с рекомендациями МАИР по программе Eurocare [15–21].
В таблице представлены сведения из базы данных популяционного ракового регистра СЗФО РФ о динамике наблюдаемой и относительной выживаемости женщин, страдающих РМЖ. Число ежегодно регистрируемых больных с 2000 по 2018 г. возросло с 4401 до 7438 (уточненные данные). Наблюдаемая выживаемость на первом году наблюдения возросла с 88,1 до 90,0 %, или на 2,2 %; относительная была практически на 2 % выше. Пятилетняя наблюдаемая выживаемость к 2014 г. достигла 62,6 %, относительная составила 69,2 %.
В отдельные годы с учетом различия возрастного состава больных этот показатель достигал 73,4 % (2012 г.).
Важно отметить существенное влияние возраста на величину показателя выживаемости. Так, однолетняя наблюдаемая выживаемость женщин в возрасте до 55 и 55 лет и старше составляла 96,1 и 88,6 % соответственно против относительной (на 1–2 % выше). Пятилетняя выживаемость больных РМЖ женщин первой возрастной группы достигла 70,5 % (в отдельные годы >75 %). Больные второй, старшей, группы в 2014 г. имели уровень 5-летней выживаемости 57,6 % (в 2012–2013 гг. >60 %).
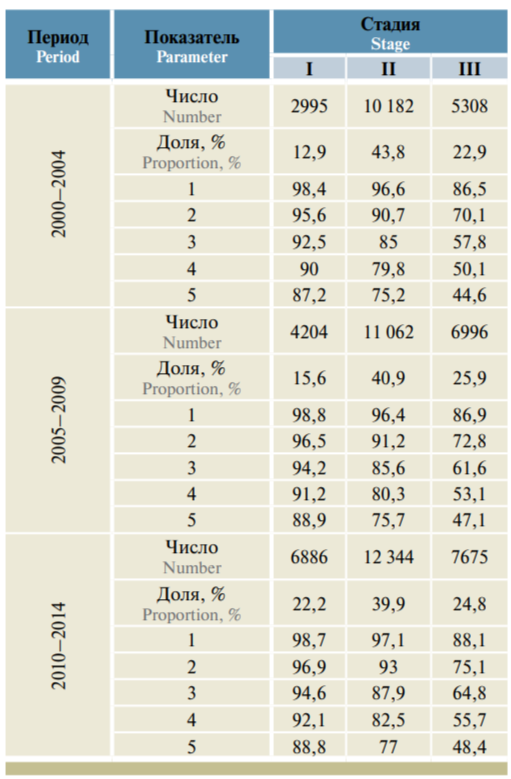
Проведенное исследование по базе данных популяционного ракового регистра СЗФО РФ показало, что больные с локализованным опухолевым процессом (I–II стадия заболевания) имеют 1- и 5-летнюю выживаемость на уровне 97,5 и 77,9 % соответственно, а больные с распространенным опухолевым процессом (III–IV стадия и больные с неуказанной стадией заболевания) в 1-й год выживают в 75–80 % случаев, за 5-летний период – в 40–42 %.
Динамика выживаемости больных РМЖ в СЗФО РФ по трем 5-летним когортам с учетом стадии заболевания отражена на рисунке 5 и в таблице 2.
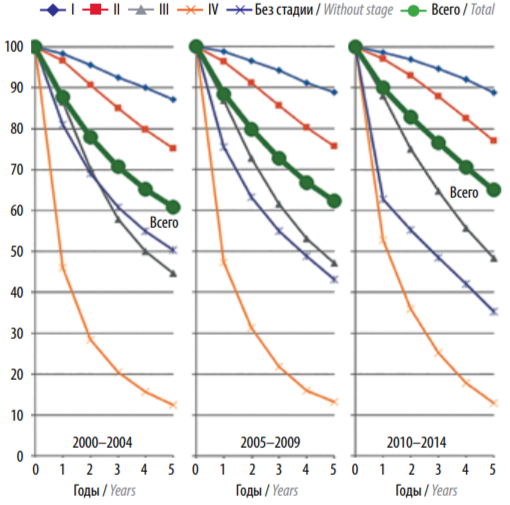
Рис. 5. Динамика наблюдаемой 5-летней выживаемости женщин, больных раком молочной железы (С50), в Северо-Западном федеральном округе с учетом стадии заболевания (база данных популяционного ракового регистра)
Всего за 3 периода наблюдения 5-летняя выживаемость больных РМЖ возросла на 6,9 %, максимальный рост выявлен среди больных с IIb–III стадией заболевания (+8,5 %) в связи с активным внедрением неоадъювантной и адъювантной системной терапии, основанной на учете молекулярно-генетических характеристик заболевания.
Согласно международным и российским рекомендациям, выделяется 4 биологических подтипа РМЖ: люминальный А, люминальный В, HER2-положительный и трижды негативный. Практикующееся в последние годы применение ингибиторов ароматазы в комбинации с ингибиторами СDK4/6 у пациентов с люминальными опухолями IIb–III стадий улучшило отдаленные результаты лечения. Так, в международном исследовании NATALEE с нашим участием применение ингибитора СDK4/6 рибоциклиба в комбинации с ингибиторами ароматазы снизило риск рецидива на 25,2 % по сравнению с только стандартной адъювантной эндокринотерапией.
У пациентов с трижды негативным РМЖ III стадии добавление к неоадъювантной химиотерапии иммунотерапии (атезолизумаб, пембролизумаб) увеличивает шанс достичь патоморфологического полного ответа (pCR) до 47 %. Особенно заметен прогресс терапии пациентов с HER2-положительным РМЖ после внедрения комбинированного таргетного лечения (трастузумаб + пертузумаб) вместе с химиотерапией. Это подтверждено в многоцентровом исследовании NeoSphere с нашим участием [22–24]. Важно обратить внимание на существенное снижение удельного веса больных, у которых стадия заболевания не была указана в медицинской документации, поступающей в базу данных популяционного ракового регистра (с 9,9 до 5,3 %).
База данных популяционного ракового регистра позволяет изучить закономерности динамики показателей выживаемости больных с учетом места проживания больных. Эти сведения представлены впервые в России (таблица 3).
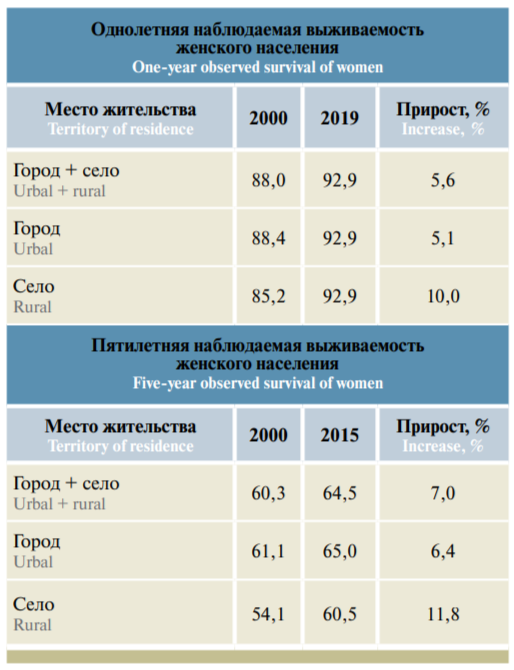
За период с 2000 по 2019 г. однолетняя наблюдаемая выживаемость больных РМЖ среди городских жителей (женское население) возросла с 88,0 до 92,9 %, или на 5,6 %, прирост показателя составил 5,1 %, а среди сельского населения – 10,0 %. К 2019 г. показатели однолетней наблюдаемой выживаемости больных РМЖ в городской и сельской местности сравнялись, относительная была на 1 % выше. Учитывая сложности в получении специализированной медицинской помощи для сельского населения, 5-летняя выживаемость женщин, страдающих РМЖ, хуже таковой городских (60,5 % против 65,0 %), однако заметно (на 11,8 %) лучше, чем в 2000 г. Относительная 5-летняя выживаемость больных на 6–7 % выше наблюдаемой.
Таким образом, проведенное исследование показало существенное увеличение заболеваемости женщин СЗФО РФ и России в целом. Отмечено негативное влияние на систему оказания специализированной помощи пандемии коронавирусной инфекции. Отражено снижение смертности женщин от РМЖ. Отмечена положительная динамика показателей наблюдаемой и относительной выживаемости больных РМЖ, определенных на основании данных популяционного ракового регистра СЗФО РФ. Впервые в России показано различие уровней выживаемости больных городской и сельской местности. Отражено воздействие проводимых клинических исследований на улучшение аналитических показателей на популяционном уровне.

1. Cancer Incidence in Five Continents. Volume XI. IARC CancerBase No. 166. Ed. by F. Bray et al. Lyon, 2021.
1. Cancer Incidence in Five Continents. Volume XI. IARC CancerBase No. 166. Ed. by F. Bray et al. Lyon, 2021.
1. Cancer Incidence in Five Continents. Volume XI. IARC CancerBase No. 166. Ed. by F. Bray et al. Lyon, 2021.
2. Злокачественные новообразования в России в 2021 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 252 с. Malignant tumors in Russia in 2021 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 252 p. (In Russ.)
2. Злокачественные новообразования в России в 2021 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 252 с. Malignant tumors in Russia in 2021 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 252 p. (In Russ.)
3. Злокачественные новообразования в России в 2000 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2002. 264 с. Malignant tumors in Russia in 2000 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2002. 264 p. (In Russ.)
4. Злокачественные новообразования в России в 2005 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2007. 252 с. Malignant tumors in Russia in 2005 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2007. 252 p. (In Russ.)
5. Злокачественные новообразования в России в 2010 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2012. 260 с. Malignant tumors in Russia in 2010 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2012. 260 p. (In Russ.)
6. Злокачественные новообразования в России в 2015 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2017. 250 с. Malignant tumors in Russia in 2015 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2016. 250 p. (In Russ.)
7. Злокачественные новообразования в России в 2016 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2016 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2017. 250 p. (In Russ.)
8. Злокачественные новообразования в России в 2017 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2017 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2018. 250 p. (In Russ.)
9. Злокачественные новообразования в России в 2018 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2019. 250 с. Malignant tumors in Russia in 2018 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 250 p. (In Russ.)
10. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 214 с. Malignant tumors in Russia in 2019 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 214 p. (In Russ.)
11. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant tumors in Russia in 2020 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
2. Злокачественные новообразования в России в 2021 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 252 с. Malignant tumors in Russia in 2021 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 252 p. (In Russ.)
3. Злокачественные новообразования в России в 2000 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2002. 264 с. Malignant tumors in Russia in 2000 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2002. 264 p. (In Russ.)
4. Злокачественные новообразования в России в 2005 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2007. 252 с. Malignant tumors in Russia in 2005 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2007. 252 p. (In Russ.)
5. Злокачественные новообразования в России в 2010 г. (заболеваемость и смертность). Под ред. В.И. Чиссова, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2012. 260 с. Malignant tumors in Russia in 2010 (morbidity and mortality). Ed. by V.I. Chissov, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2012. 260 p. (In Russ.)
6. Злокачественные новообразования в России в 2015 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2017. 250 с. Malignant tumors in Russia in 2015 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2016. 250 p. (In Russ.)
7. Злокачественные новообразования в России в 2016 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2016 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2017. 250 p. (In Russ.)
8. Злокачественные новообразования в России в 2017 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2017 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2018. 250 p. (In Russ.)
9. Злокачественные новообразования в России в 2018 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2019. 250 с. Malignant tumors in Russia in 2018 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 250 p. (In Russ.)
10. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 214 с. Malignant tumors in Russia in 2019 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 214 p. (In Russ.)
11. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant tumors in Russia in 2020 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
12. Мерабишвили В.М. Состояние онкологической помощи в России: рак молочной железы среди женского населения. Заболеваемость, смертность, достоверность учета, детальная локализационная и гистологическая структура (популяционное исследование на уровне федерального округа). Вопросы онкологии 2022;68(3):291. Merabishvili V.M. The state of oncological care in Russia: breast cancer among the female population. Morbidity, mortality, accounting reliability, detailed localization and histological structure (population study at the federal district level). Voprosy onkologii = Oncology Issues 2022;68(3):291. (In Russ.)
13. Мерабишвили В.М. Аналитические показатели индекса достоверности учета. Вопросы онкологии 2018;64(3):445–52. Merabishvili V.M. Analytical indicators of index of accuracy. Voprosy onkologii = Oncology Issues 2018;64(3):445–52. (In Russ.)
2. Злокачественные новообразования в России в 2021 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 252 с. Malignant tumors in Russia in 2021 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 252 p. (In Russ.)
6. Злокачественные новообразования в России в 2015 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2017. 250 с. Malignant tumors in Russia in 2015 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2016. 250 p. (In Russ.)
7. Злокачественные новообразования в России в 2016 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2016 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2017. 250 p. (In Russ.)
8. Злокачественные новообразования в России в 2017 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2017 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2018. 250 p. (In Russ.)
9. Злокачественные новообразования в России в 2018 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2019. 250 с. Malignant tumors in Russia in 2018 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 250 p. (In Russ.)
10. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 214 с. Malignant tumors in Russia in 2019 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 214 p. (In Russ.)
11. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant tumors in Russia in 2020 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
2. Злокачественные новообразования в России в 2021 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2022. 252 с. Malignant tumors in Russia in 2021 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2022. 252 p. (In Russ.)
6. Злокачественные новообразования в России в 2015 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2017. 250 с. Malignant tumors in Russia in 2015 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2016. 250 p. (In Russ.)
7. Злокачественные новообразования в России в 2016 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2016 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2017. 250 p. (In Russ.)
8. Злокачественные новообразования в России в 2017 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2018. 250 с. Malignant tumors in Russia in 2017 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2018. 250 p. (In Russ.)
9. Злокачественные новообразования в России в 2018 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2019. 250 с. Malignant tumors in Russia in 2018 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, G.V. Petrova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 250 p. (In Russ.)
10. Злокачественные новообразования в России в 2019 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2020. 214 с. Malignant tumors in Russia in 2019 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2019. 214 p. (In Russ.)
11. Злокачественные новообразования в России в 2020 г. (заболеваемость и смертность). Под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой. М.: Московский научно-исследовательский онкологический институт им. П.А. Герцена – филиал ФГБУ «Национальный медицинский исследовательский центр радиологии» Минздрава России, 2021. 252 с. Malignant tumors in Russia in 2020 (morbidity and mortality). Ed. by A.D. Kaprin, V.V. Starinskiy, A.O. Shakhzadova. Moscow: P. Hertzen Moscow Oncology Research Institute – branch of the National Medical Research Radiology Center, Ministry of Health of Russia, 2021. 252 p. (In Russ.)
12. Мерабишвили В.М. Состояние онкологической помощи в России: рак молочной железы среди женского населения. Заболеваемость, смертность, достоверность учета, детальная локализационная и гистологическая структура (популяционное исследование на уровне федерального округа). Вопросы онкологии 2022;68(3):291. Merabishvili V.M. The state of oncological care in Russia: breast cancer among the female population. Morbidity, mortality, accounting reliability, detailed localization and histological structure (population study at the federal district level). Voprosy onkologii = Oncology Issues 2022;68(3):291. (In Russ.)
13. Мерабишвили В.М. Аналитические показатели индекса достоверности учета. Вопросы онкологии 2018;64(3):445–52. Merabishvili V.M. Analytical indicators of index of accuracy. Voprosy onkologii = Oncology Issues 2018;64(3):445–52. (In Russ.)
14. Мерабишвили В.М. Индекс достоверности учета – важнейший критерий объективной оценки деятельности онкологической службы для всех локализаций злокачественных новообразований, независимо от уровня летальности больных. Вопросы онкологии 2019;65(4):510–5. Merabishvili V.M. Index of accuracy – the main criteria for an objective assessment of the activity of the oncological service for all localities of malignant tumors, regardless of the level of lethality of patients. Voprosy onkologii = Oncology Issues 2019;65(4):510–5. (In Russ.)
15. Мерабишвили В.М. Выживаемость онкологических больных. Выпуск 2. Часть I. Под ред. Ю.А. Щербука. СПб.: ООО «Издательско-полиграфическая компания «КОСТА», 2011. 332 с. Merabishvili V.M. Survival of cancer patients. Issue two. Part I. Ed. by Yu.A. Shcherbuk. Saint Petersburg: LLC “KOSTA”, 2011. 332 p. (In Russ.)
16. Мерабишвили В.М. Выживаемость онкологических больных. Выпуск 2. Часть II. Под ред. Ю.А. Щербука. СПб.: ООО «Издательско-полиграфическая компания «КОСТА», 2011. 408 с. Merabishvili V.M. Survival of cancer patients. Issue two. Part II. Ed. by Yu.A. Shcherbuk. Saint Petersburg: LLC “KOSTA”, 2011. 408 p. (In Russ.)
17. Survival of cancer patients in Europe: the EUROCARE Study (IARC Scientific Publications No. 132). Ed. by F. Berrino et al. Lyon: International Agency for Research on Cancer, 1995.
18. Survival of cancer patients in Europe: the EUROCARE-2 study (IARC Scientific Publications No. 151). Ed. by F. Berrino et al. Lyon: International Agency for Research on Cancer, 1999.
19. Berrino F., Capocaccia R., Esteve J. et al. EUROCARE-3: the survival of cancer patients diagnosed in Europe during 1990–94. Ann Oncol 2003;14(Suppl 5):1–155.
20. Capocaccia R., Gavin A., Hakulinen T. et al. Survival of cancer patients in Europe, 1995–2002. The EUROCARE-4 study. Eur J Cancer 2009;45.
21. De Angelis R., Sant M., Coleman M. et al. Cancer survival in Europe 1999–2007 by country and age: results of EUROCARE-5 – a population-based study. Lancet Oncol 2014;15:23–34. DOI: 10.1016/ S1470-2045(13)70546-1
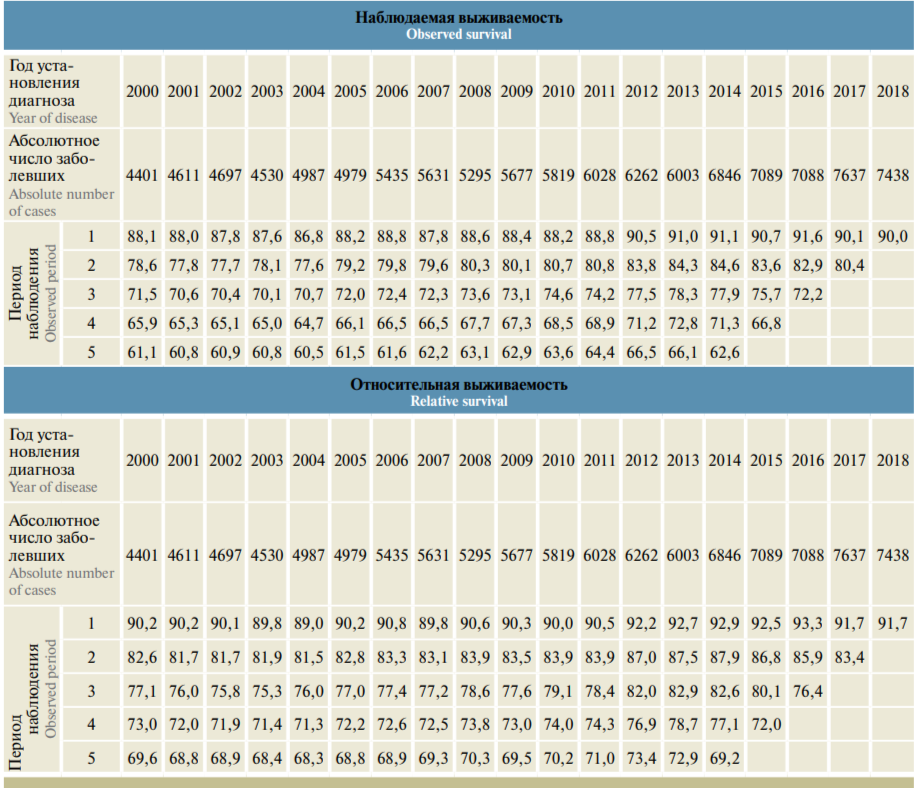
Таблица 1. Наблюдаемая и относительная выживаемость женщин, больных раком молочной железы (С50), в Северо-Западном федеральном округе России (база данных популяционного ракового регистра)
Таблица 2. Динамика наблюдаемой 5-летней выживаемости женщин, больных раком молочной железы (С50), за 2000–2014 гг. в Северо-Западном федеральном округе с учетом стадии заболевания (база данных популяционного ракового регистра)
22. Семиглазов В.Ф., Криворотько П.В., Семиглазов В.В. и др. Органосохраняющее, реконструктивное и системное лечение рака молочной железы. М.: СИМК, 2022. Semiglazov V.F., Krivorotko P.V., Semiglazov V.V. et al. Organpreserving, reconstructive and systemic treatment of breast cancer. M.: SIMK, 2022. (In Russ.)
23. Gianni L., Semiglazov V.F., Viale G. et al. Pathologic complete response (pCR) to neoadjuvant treatment with or without atezolizumab in triple negative? Early high-risk and locally advanced breast cancer. NeoTRIPaPDL1 Michelangelo randomized study. SABCC 2019.
24. Gianni L., Pienkowski T., Im Y.H. et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-posistive breast cancer (NeoSphere): A randomized multicenter, open-lable, phase 2 trial. Lancet Oncol 2012;13:25–32.
Таблица 3. Однолетняя и 5-летняя выживаемость больных раком молочной железы в Северо-Западном федеральном округе с учетом территории проживания жителей